2019年9月20日,上海科技大学免疫化学研究所特聘教授姜标教授团队在Journal of Medicinal Chemistry发表题为Discovery of SIAIS178 as an effective BCR-ABL degrader by recruiting von Hippel-Lindau (VHL) E3 Ubiquitin Ligase的文章,详细介绍了靶向降解BCR-ABL融合蛋白的PROTAC小分子SIAIS178的发现,并探究了其用于白血病治疗的可行性。
慢性髓性白血病(CML)是造血干细胞克隆性增殖引发的恶性肿瘤,约占成人白血病的15%。染色体异位融合蛋白BCR-ABL是慢性粒细胞白血病发病的关键驱动因素,目前已有包括伊马替尼、达沙替尼等在内的多个靶向BCR-ABL的酪氨酸激酶小分子抑制剂应用于临床。尽管这些酪氨酸激酶抑制剂在BCR-ABL+慢性髓性白血病中疗效显著,但一方面病人需要长期甚至终生服药,经济负担较大;另一方面临床耐药亦成为CML治疗中面临的巨大挑战。因此,将BCR-ABL彻底敲除或者降解被认为是更加有效的新型治疗策略之一。
蛋白靶向降解 (targeted protein degradation) 是药物研发领域的一个新兴方向,靶向蛋白嵌合体 (proteolysis targeting chimera, PROTAC)是其中最受关注的技术。研究表明PROTAC技术与当前小分子激酶抑制剂药物相比,具有延缓克服耐药、靶向不可成药靶点、提高选择性等诸多优势。此前,耶鲁大学Craig M. Crews教授基于第二代BCR-ABL抑制剂达沙替尼和VHL-1配体构建了PROTAC小分子Dasa-6-2-2-6-VHL,但对于目标蛋白BCR-ABL并没有降解作用。
本课题组研究人员以达沙替尼为靶蛋白配体,通过本课题组设计的E3泛素连接酶配体库VHL-1相连,进而筛选优化得到了PROTAC小分子SIAIS178。体内外功能实验研究发现,SIAIS178在体外对BCR-ABL+依赖的白血病细胞具有显著的生长抑制活性,并呈现很好的选择性,在体内小鼠动物模型中亦呈现出显著的抗白血病活性(图1)。机制研究表明SIAIS178可以诱导靶蛋白BCR-ABL与VHL E3泛素连接酶之间形成稳定的三元复合物(图2),进而实现对BCR-ABL蛋白的显著降解。此外,SIAIS178还能有效降解临床上与伊马替尼和达沙替尼耐药相关的多种耐药突变体形式。进一步地,研究人员通过将小分子抑制剂达沙替尼与小分子降解剂SIAIS178(化合物19)同时给药一段时间后再予以撤药观察,发现SIAIS178在体外表现了更加持久的细胞增殖抑制和诱导凋亡活性。该研究成果表明PROTAC降解技术在治疗BCR-ABL+白血病及克服临床耐药问题上具有潜在的应用价值。
此项工作上科大免疫化学研究所博后赵全菊、2019级博士生任超伟及免疫化学研究所博后刘林义为共同第一作者,姜标教授课题组助理研究员杨小宝(进行PROTAC设计及其合成工作)及助理研究员阴倩倩(进行了化合物的药效及机制研究工作)为共同通讯作者。课题开展过程中,免疫化学研究所抗体结构学实验室杨贝副研究员及助理研究员徐有伟提供协助,成功验证了体外PROTAC小分子三元复合物的形成。该研究得到了国家自然科学基金、上海市科委基金、上海市扬帆计划及中国博士后科学基金和和径医药科技(上海)有限公司的支持。
上海科技大学免疫化学研究所特聘教授姜标课题组目前致力于蛋白降解药物PROTAD(proteolysis targeting drug)技术平台构建以及抗肿瘤药物及免疫调节药物的开发,已经申请相关专利达10项之多。本次成果的发表是前期工作基础上取得的阶段性进展,亦为后续的工作奠定了良好的基础。
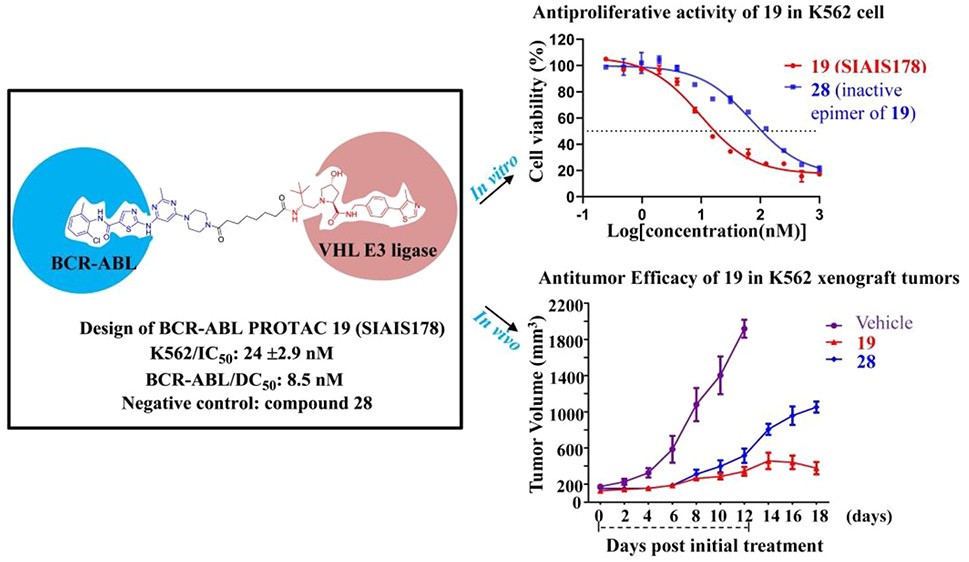
Figure 1. SIAIS178(化合物19)体内体外抗白血病活性。化合物28为化合物SIAIS178的阴性对照物
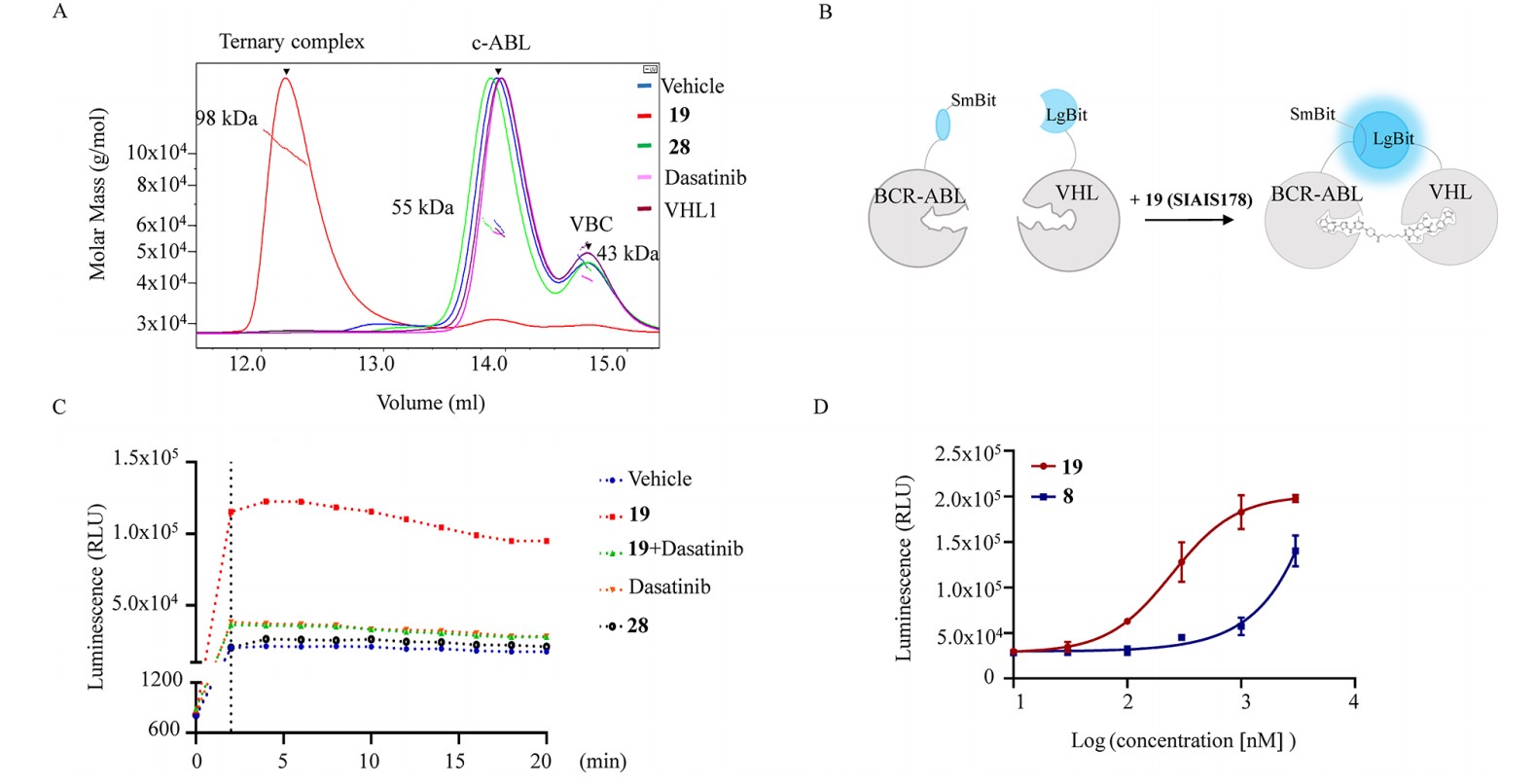
Figure 2. SIAIS178(化合物19)诱导BCR-ABL和VHL形成三元复合物 (A) SIAIS178引起重组ABL蛋白(激酶域)与重组VHL/EloB/EloC (VBC)蛋白形成三元复合物;(B) NanoBiT蛋白互补实验示意图;(C)不同化合物在NanoBiT蛋白互补实验中的荧光-时间关系图;(D) 不同化合物在NanoBiT蛋白互补实验中的荧光-浓度关系图。化合物28为化合物SIAIS178的阴性对照物, VHL1为E3泛素化酶VHL配体。
文章链接:https://pubs.acs.org/doi/10.1021/acs.jmedchem.9b01264



