10月22日,国际一流学术期刊10月22日,国际一流学术期刊Nature Protocols(2014年度影响因子:9.673)在线发表了我校免疫化学研究所(SIAIS)抗体化学实验室的最新研究成果“Efficientdelivery of nuclease proteins for genome editing in human stem cells andprimary cells”。
在这篇论文中,副研究员刘佳及其同事报道了基于核酸酶蛋白质的基因编辑新技术。和传统方法相比,将蛋白质运输进细胞直接进行基因编辑,能使核酸酶快速发挥活性,并减少基因组DNA暴露在核酸酶中的时间,从而在实现高效靶向基因编辑的同时,降低基因编辑的细胞毒性及“脱靶”效应。这项新技术的发明将对基因编辑用于临床治疗起到显著的推动作用。 位点特异性核酸酶是高效的基因编辑工具,三种核酸酶技术(ZFN、TALEN、CRISPR/Cas9)的出现和发展为生物科学研究带来了重要变革,同时也为基因相关疾病的治疗提供了新思路。但是,要使基因编辑技术得到更广泛的应用,特别是用于临床治疗,则需要安全、高效的方法将核酸酶运输进细胞内。传统方法中,核酸酶是以DNA或mRNA形式被运输到细胞中,然后依靠细胞自身的转录、翻译机器产生有活性的核酸酶蛋白质。 基于核酸酶蛋白质的基因编辑技术由斯克利普斯研究所(TheScripps Research Institute)的CarlosF. Barbas III(已故)研究组率先报道。Barbas教授生前是我校免疫化学研究所的特聘教授。 文章通讯作者、并列第一作者(排在第一)刘佳副研究员在Barbas实验室攻读博士后期间对此技术进行了优化及拓展。“同很多重大的研究发现类似,这个技术是在一次组会集体讨论过程中碰撞出的火花,”刘副研究员回忆到,“结果令人没有想到的是,当用ZFN进行测试时发现,这个蛋白质自身就能高效穿过细胞膜并对基因组进行高效基因编辑”。 他在后续研究中对ZFN进行了蛋白质工程改造,使其在CD4+T细胞中的基因编辑效率得到大幅提升,期望这项技术能用于艾滋病的基因治疗。他还发明了一种新方法用于将TALEN蛋白质运送到细胞中,这种方法通过化学偶联将细胞穿膜肽共价连接到TALEN蛋白质上,赋予其穿膜能力。他还将继续研发此项技术,希望能实现对TALEN核酸酶的细胞特异性运输。和前两者不同,Cas9核酸酶及其单链RNA(sgRNA)的复合物则是通过核转染方式运输到细胞中。 在这篇最新报道中,刘副研究员及其同事用ZFN和Cas9核酸酶蛋白质在CD4+T细胞和胚胎干细胞中分别实现了25%及33%的基因编辑效率。“通过进一步优化,我们现在已能在CD4+T细胞和胚胎干细胞中分别实现39%及65%的基因编辑效率”,他补充道。高效的靶向基因编辑及显著提高的安全性使得核酸酶蛋白质成为精准基因编辑的有效工具。 本研究的合作单位包括美国斯克利普斯研究所、韩国首尔基础科学研究所、意大利EdmundMach基金会、韩国首尔国立大学。
文章链接:Efficient delivery of nucleaseproteins for genome editing in human stem cells and primary cells
(DOI:10.1038/nprot.2015.117)
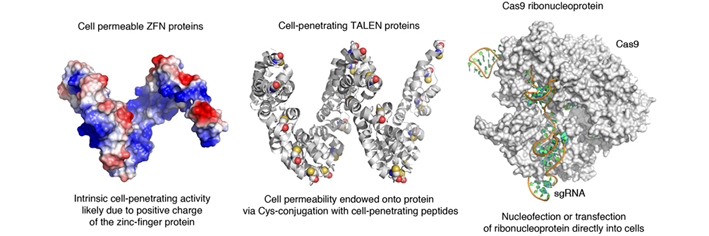
核酸酶蛋白质运输入细胞的三种模式 我校作者合影。左起:2013级研究生王楠(第四作者)、副研究员刘佳(并列第一作者)、 博士后杨异凤(第三作者)、2014级研究生水赛兰(第五作者)



