2019年开年不到1个月,我校迎来“开门红”――北京时间1月25日凌晨,国际顶尖期刊《Cell》同时发表了上海科技大学的两项重大科研成果,分别是:上科大免疫化学研究所领衔的科研团队率先在国际上成功解析分枝杆菌关键药靶蛋白MmpL3以及“药靶─药物”复合物的三维空间结构,揭示了创新药物杀死细菌的全新分子机制,为今后新型抗生素的研发开辟了一条全新路径;上科大iHuman研究所领衔的科研团队首次成功解析了人源大麻素受体CB2与新型拮抗剂复合物的三维精细结构,揭示了配体对受体的精细调控方式,为免疫调节类疾病、炎性神经痛、肿瘤等疾病的药物研发提供了非常重要的结构理论基础。
免疫化学研究所研究团队解析分枝杆菌关键药靶蛋白结构,开辟抗生素研发全新途径
结核分枝杆菌,是引起结核病的病原菌,可侵犯全身各器官,尤以肺结核为最多见。至今,结核病仍为重要的传染病之一。尽管在上个世纪中叶,链霉素的发现结束了几千年来结核杆菌肆虐人类生命的历史,此后科学家们又开发了异烟肼、利福平等有效药物,然而近年来,艾滋病与结核病的交叉感染以及药物的不合理使用,导致了耐药结核病的产生,再次成为危害全球公共卫生的严重问题。据统计,全世界目前仍有约1/3的人口被结核杆菌感染。世界卫生组织近期发布的《全球结核病报告》显示,2017年全球结核病患者死亡人数约为160万,新发结核病患者约1000万,在感染性疾病中堪称“头号杀手”。因此,针对结核分枝杆菌新药靶点的发现以及新药的研发迫在眉睫。
不同于其他细菌,作为一种分枝杆菌,结核杆菌的细胞表面有一层非常致密的细胞壁,而分枝菌酸就是这层细胞壁的主要成分之一。由于分枝菌酸的存在,结核杆菌不仅可以免受许多化学物质的侵蚀,还可以耐受很多常见的抗生素。不过,再可怕的敌人也有致命弱点,结核杆菌也不例外。结核杆菌赖以生存的分枝菌酸,其合成与运输的过程恰恰就是它的致命弱点。最近,科学家们发现分枝杆菌中有一种被称为“MmpL3”的膜蛋白在分枝菌酸的制造过程中起了关键作用。它负责把细菌在细胞内合成的分枝菌酸前体转运到细胞膜外,这些前体物质会被进一步加工合成为分枝菌酸。因此,MmpL3蛋白在分枝菌酸合成通路中起到了一台“传送机”的作用。这台“传送机”的动力来源于膜外侧的质子向膜内侧流动形成的质子流。这股质子流就像水流发电一样,给这台“传送机”提供了源源不断的动力。鉴于MmpL3对分枝杆菌至关重要的地位,它已成为抗结核新药研发的一个关键靶标。目前,有报道称国际制药公司利用高通量技术筛选获得的抗结核新药SQ109(已完成临床II-III期试验)可能靶向MmpL3。但是,这台“传送机”的构造仍然是一个谜,科学家们对临床抗结核药物SQ109如何靶向MmpL3的分子机制更是一无所知。这些都成为了抗结核新药研发中的国际难题。
免疫化学研究所特聘教授饶子和院士的科研团队一直致力于针对结核杆菌的新药靶点研究及新药研发。2018年10月25日,研究团队解析了分枝杆菌能量代谢系统呼吸链超级复合物的高分辨率冷冻电镜结构,在呼吸链领域取得了重要突破,以研究长文(Research Article)的形式在国际顶尖期刊《Science》上发表。在此基础上,该研究团队继续打响了抗结核杆菌新药研发的“攻坚战”。为了揭示分枝杆菌中关键药靶蛋白MmpL3的工作机制和阐明临床药物SQ109的杀菌机理,历经近6年的漫长时光,研究团队先后克服了样品量少、稳定性差以及晶体生长和衍射等一系列难题,最终利用X-射线晶体衍射技术,成功解析了MmpL3蛋白及其与多种候选药物复合物在原子分辨率水平的三维空间结构,破解了这台“传送机”工作的奥秘和候选药物的杀菌机制。
研究发现,MmpL3蛋白可分为膜外、跨膜和细胞内三个部分。同时,研究人员还捕捉到这台“传送机”在输送底物(分枝菌酸合成前体类似物)时的状态,首次描绘了其在工作状态的三维图像。不仅如此,研究团队还分别解析了MmpL3蛋白与三种抑制剂(SQ109、AU1235和ICA38)复合物三维空间结构,揭开了SQ109如何进攻MmpL3蛋白使其失活、杀死细菌之谜。研究发现,SQ109等抑制剂小分子都靶向MmpL3蛋白的跨膜区,“封闭”该蛋白的质子内流通道,破坏MmpL3工作时的能量供给,直接造成这台“传送机”的“瘫痪”。为了设计更有效的抑制剂,研究团队还利用计算机“虚拟筛选”技术,对成药库的药物分子进行了筛选。研究人员惊奇地发现,一种曾经在市场上销售的减肥药利莫那班(rimonabant)竟有可能是MmpL3蛋白的抑制剂。更令人不可思议的是,利莫那班是全球首个针对人源大麻素受体CB1的拮抗剂,很难想象靶向人类蛋白受体的药物也可以杀死结核杆菌。随后研究团队又解析了利莫那班与MmpL3蛋白复合物的三维结构,从而证实了这一结论。该结构显示,利莫那班同样“神奇”地堵住了MmpL3的质子内流通道。但是,这种结合模式既不同于上述SQ109等抑制剂的结合方式,与“利莫那班-CB1受体”的结合模式也是大相径庭。
据饶子和院士介绍,MmpL3蛋白隶属于RND(Resistance, Nodulation and Division)蛋白质超家族。这类蛋白质广泛存在于各种病原菌中,不过它们主要扮演着“药泵”的角色。当细菌摄入抗生素后,这类家族的蛋白质就开始工作,负责把细菌胞内的抗生素排出胞外。因此,这类蛋白质也往往是病原体对抗生素耐药的罪魁祸首。有趣的是,尽管RND蛋白质超家族的成员们形形色色,长相也不尽相同,但它们都通过质子内流获取能量、行使功能。本研究首次勾勒出药物分子如何精确制导“打击”引发细菌耐药的蛋白质超家族成员关键活性部位的三维图像,其意义在于不仅为由分枝杆菌引起的疾病(结核病、麻风病等)的药物研发奠定了重要的理论基础,更为新型抗生素的研发、解决全球日趋严重的抗生素耐药问题开辟了一条全新途径。
谈及这个课题的研究历程,论文第一作者张兵百感交集:6年来的研究过程对研究人员的体力、毅力和心理承受能力,都是一个大考验。很多时候我们满怀希望、通宵达旦地在上海光源开展实验,衍射了成百上千颗的蛋白质晶体,但却无法获得一套可供开展后续工作的数据,信心几近崩溃。由于课题的难度极大,也曾想过放弃。但每当脑海里浮现出这个念头时,饶老师对我的谆谆教诲就在耳边萦绕“结核病是一个穷人病,我们国家是结核病主要负担国之一,由于利润低,很多知名的药物公司都停止了抗结核药物的研发,我们作为一名科研工作者,要义不容辞地把这个担子挑起来!”师长的期望给予了我很大鼓励,使我在科研道路上坚持不懈、初心不改。作为上海科技大学的学子,“立志、成才、报国、裕民”的育人理念已经深深烙在我们每个上科大人的心里,激励着我为研发有自主知识产权的抗结核药物一如既往、攻坚克难,贡献自己一份力量。通过一次次认真总结和创新尝试,“屡战屡败、屡败屡战”,功夫不负有心人,直至此次我们团队终于攻克了这个世界性难题。当饶老师通知我论文被《Cell》杂志接受的时候,他语重心长地说“今晚你终于可以睡个好觉了”。那一刻我激动得热泪盈眶,感慨自己这一路走来的不易,感激研究团队对自己的帮助,感谢学校对自己的支持。
上述成果以“Crystal structures of membrane transporter MmpL3, an anti-TB drug target”为题,在《Cell》上发表。上海科技大学2013级硕博连读研究生张兵为论文第一作者,免疫化学研究所副研究员李俊为论文的并列第一作者兼共同通讯作者,免疫化学研究所研究员杨海涛、特聘教授饶子和院士为共同通讯作者。上科大为第一完成单位。本项研究由多家科研单位联合攻关、协作完成。上海科技大学免疫化学研究所姜标教授,iHuman研究所刘志杰教授和中科院上海药物研究所蒋华良院士参与了此项研究,同时,该工作获得了上海科技大学生命科学与技术学院的大力支持,国家蛋白质科学中心(上海)和中科院生化细胞所提供了技术支持。
iHuman研究所科研团队解析人源大麻素受体CB2结构,为药物设计开启新篇章
iHuman研究所刘志杰教授的科研团队在人体细胞信号转导研究领域再获重大突破,成功解析了人源大麻素另一个受体CB2 (human cannabinoid receptor 2)的三维精细结构,揭示了小分子拮抗剂与CB2的结合及调控方式。
桑科大麻属植物大麻(学名:Cannabis sativaL.)被用于生活、医药、宗教和娱乐已有数千年历史。我国是种植和使用大麻最早的国家,早期药书《神农本草经》及《本草纲目》中就有关于大麻的医药和保健用途的大量记载。植物大麻中含有几十种有效成份,比较有名的致幻成份―“四氢大麻酚”(∆9-tetrahydrocannabinol, THC)主要作用于人体中的大麻素受体CB1和CB2。CB1分布于全身,也是中枢神经系统中分布最广的G蛋白偶联受体(G protein-coupled receptor,GPCR)之一,而CB2则主要存在于人的免疫系统中,中枢神经系统中也有少量分布。CB2是治疗免疫调节类疾病、炎性神经痛、神经性炎症和神经退行性疾病等的重要靶点。最近的研究显示,CB2的拮抗剂在治疗肾纤维化、延缓肿瘤发展等方面具有较好疗效。尽管CB1与CB2之间氨基酸序列的同源度高达44%,但两个受体无论在体内分布还是在调控的生理功能上均存在较大差异。揭示CB2的三维精细结构及与配体分子的相互作用机制,以及其与CB1在协同调节人体内源性大麻素系统中的相互关系,既是一个重要的科学问题,也是一项对众多疾病的新药研发具有重要意义的科学实践。
过去五年中,刘志杰课题组试图理解大麻素受体调控的重要生理功能和其结构基础。目前,研究团队已分别发表了CB1与拮抗剂AM6538复合物的晶体结构(Cell, 2016)、CB1分别与激动剂AM841及AM11542复合物的晶体结构(Nature, 2017)。在前期工作的基础上,为攻克CB2受体结构及调控机制,研究团队首先通过突变位点预测和大量表达载体筛选,经过多轮反复优化获得了高质量的CB2蛋白样品,然而产生出的晶体衍射能力较弱。为了提高晶体衍射质量,研究团队又进一步筛选了几十个不同来源的小分子配体,并与美国东北大学的Alexandros Makriyannis教授团队合作设计了CB2新型拮抗剂AM10257,最终获得衍射能力超过3Å的棒状晶体。由于晶体各向异性比较严重,即晶体在一个方向衍射能力较强而长轴方向衍射能力相对较弱,这给数据处理和结构解析带来很大挑战。为了克服这一困难,研究团队对实验策略进行了调整和优化,对收集到的大量衍射数据同时进行严格筛选和分类,最终成功解析了CB2与AM10257复合物2.8埃分辨率的晶体结构。该结构清晰展示了拮抗剂AM10257与CB2的相互作用模式,通过与CB1三维结构的比对分析,发现同处于拮抗状态下的CB2与CB1不但结构差别极大,拮抗状态的CB2-AM0257结构反而与激动剂结合的CB1-AM11542结构具有更高的相似性。受此启发,该团队检测了AM10257对CB1的调控作用,不出意外地发现,AM10257对CB1确实表现出了弱激动剂的功能。“一种配体对同一GPCR家族中不同成员具有相反调控作用的例子具有非常高的研究价值,”刘志杰教授说,“CB1和CB2两种受体间的这种阴阳平衡关系是否对人体生理功能的精确调控具有特殊的生理意义,是一个值得我们进一步深入探究的重要科学问题”。
这次研究成果也是iHuman研究所科研团队继成功揭开了大麻素受体CB1的“阴阳双面”后,在大麻素受体系列研究中的又一重大突破。该研究成果将极大推动靶向大麻素受体CB1和CB2的特异探针设计,实现对人体内非常重要的大麻素系统的精准调控,为探究众多疾病的发生和发展机理以及靶向性新药的研发具有重要意义。
为了这项课题,文章第一作者李潇婷在临近毕业之时主动选择了延期,回首这段“柳暗花明又一村”的艰难往事,李潇婷感慨道:“我研究的CB2受体作为GPCR家族的成员之一,一方面不能使用高压破碎、超声等快速省力的方法提取其蛋白;但另一方面GPCR本身的不稳定性,还需要进行一轮又一轮的克隆改造和优化。为了早点获得结果,早起和熬夜成为生活日常,正是应了江校长在开学典礼上对我们首届研究生的寄语:‘做得了钢铁侠,坐得起冷板凳’。经常性的挫败,有时会让自己觉得这种漫长的努力和等待或许是一种无谓的坚持。但也许老天总是会在你感到无望时给你一点点希望。2016年3月,距离自己正常毕业还有两年的时候,我的坚持终于得到了回报,获得了CB2受体的蛋白晶体,那时感觉自己攻克CB2受体结构在即,按时毕业在望。然而之后接近半年的晶体优化却没有任何进展,衍射分辨率仍然在10Å徘徊。到底是坚持使用同一克隆继续优化晶体,还是重新再来一轮克隆优化?到底是发表暂时的成果按时毕业,还是选择放弃重头开始?经过审慎考虑,我选择了后者。做科研不但需要坚持,有时更需要理智地割舍。现在回想起来,正是当时的‘不将就’,才成就了今天的圆满。”
华甜副研究员评价道:“人体的内源性大麻素系统是一个非常神奇的调控系统,它参与很多生理过程的调控且与众多疾病密切相关。我们在研究过程中不断发现它令人意外的奇妙特性。目前我们的研究已经深入到更加复杂的下游信号转导机制和相关的药物研发上。非常希望我们努力的成果能为人类健康做一份贡献”。
该成果以“Crystal Structure of the Human Cannabinoid Receptor CB2”为题,在《Cell》上发表。上科大2013级硕博连读研究生李潇婷、iHuman研究所副研究员华甜为论文共同第一作者,iHuman研究所执行所长、生命学院教授刘志杰为通讯作者,上科大为第一完成单位。参与该项研究的还有iHuman研究所创始所长Raymond Stevens教授课题组、iHuman研究所研究员、生命学院助理教授赵素文课题组及美国东北大学、美国斯克利普斯研究所、美国南加州大学、美国国立卫生研究院和俄罗斯莫斯科物理技术学院等单位科研人员。iHuman研究所基因克隆平台、真核细胞表达平台、蛋白纯化平台、功能研究平台的工作人员为该项研究提供了强大的技术支持。
首批硕博连读研究生“勇挑大梁”两大研究所协力攻坚:教学与科研同步“丰收”
此次同期亮相《Cell》的科研成果,在许多环节上有着非常奇妙的关联度和巧合点。
首先是科研团队,免疫化学研究所和iHuman研究所同为学校聚焦生命科学领域的兄弟研究所;
其次是科研场地,两个研究所都位于同一驻地――“人字楼”,二者比邻而居;
再次,比地理位置上的巧合更为奇妙的是,“利莫那班”(Rimonabant)本是针对人源大麻素受体CB1的拮抗剂类减肥药,此次,免化所科研团队同时发现它也是一种针对结核杆菌蛋白MmpL3的抑制剂。这种科学上出乎意料的天然联系把“同一屋檐下”的两个研究所结合得更加紧密,使得两个研究机构之间在学术上充分交融、在信息上互通有无、在科研上携手共进。此次两篇论文同期亮相,可谓“同源共生结硕果,双花并蒂开门红”。
最值得一提的是,这两篇重量级学术论文的第一作者都是我校招收的首批硕博连读研究生。iHuman研究所博士研究生李潇婷同学认为,是学校丰富的科研资源、先进的指导模式及国际化的培养理念造就了自己。李潇婷提到一个细节,5年多前参加面试时,自己还只能用蹩脚的英语和创始所长Raymond Stevens对话。而现在,她已经能够自信、流利地在各类国际会议中向国内外学者讲解自己的科研成果。求学期间,李潇婷还曾得益于学校为学生提供赴海外进行国际交流学习锻炼的机会:到瑞士光源参加技术培训、到美国波士顿参加国际学术会议,经常参与国际合作单位的联合组会……这些对她后来的成长发展起到了很大的帮助,也为她今天取得的成果打下了重要的基础。
免疫化学研究所博士研究生张兵则表示,衷心感谢学校提供了优越的科研环境和学习条件,特别是学校服务国家经济社会发展战略的办学使命和宗旨,对坚定自己的科研道路起到了深刻影响。免化所作为国际化高水平的研究机构,凭籍着优质的研究团队、先进的科研设备、完备的后勤保障和独特的管理模式,确保了高水平的研究成果和高效率的科研转化不断涌现,在国际上的影响力不断增强。每年,学校举办的免疫化学国际生物论坛都会吸引来自国内和国际众多专家,学者和企业代表的积极参与。
目前,上科大共有一届本科生、三届硕士研究生及一届博士研究生顺利毕业。自2013年首批硕博连读研究生入学以来,截至2018年12月,398名硕博连读研究生共发表期刊论文和会议论文607篇,其中影响因子10以上的期刊论文和顶会论文等高水平成果114篇。
2016年4月15日,国务院发布上海科创中心建设方案,明确指出上科大在上海张江综合性国家科学中心建设中将承担重要任务。目前,学校正与中科院上海分院科研院所等单位合作,负责或参与建设软X射线自由电子激光用户装置、活细胞结构与功能成像等线站、超强超短激光实验装置、光源二期,牵头硬X射线自由电子激光装置的建设并承担多项科创中心建设重点工作。截至2018年12月,学校的五个学院、三个研究所已经建立了224个研究组,科研工作全面展开。例如,利用光能在室温下把甲烷一步转化为液态产品(2018年7月,《Science》)、人源卷曲受体(Frizzled-4)的结构与功能研究(2018年8月,《Nature》)、五羟色胺2C受体三维结构解析(2018年2月,《Cell》)、人源大麻素受体结构解析(2017年7月,《Nature》;2016年10月,《Cell》)、人源胰高血糖素样肽-1受体晶体结构解析(2017年5月,《Nature》)等高水平科研成果正在不断涌现。这些科研突破也是上海科创中心在基础科学研究方面的重大成果。
免疫化学研究所成果、分枝杆菌药靶蛋白MmpL3相关文章链接:
https://www.cell.com/cell/fulltext/S0092-8674(19)30036-4
iHuman研究所成果、CB2结构相关文章链接:
https://www.cell.com/cell/fulltext/S0092-8674(18)31625-8
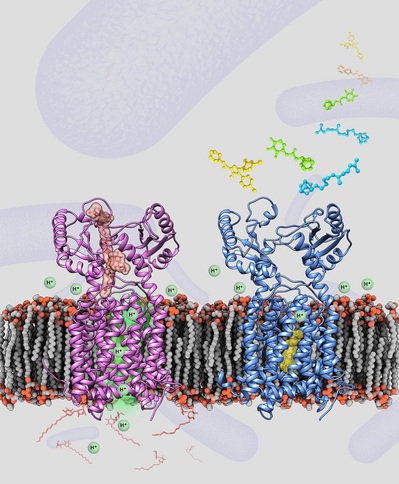
图注:分枝杆菌药靶蛋白MmpL3结合底物类似物的结构(左)和MmpL3蛋白与抗结核临床药物SQ109的复合物结构(右)
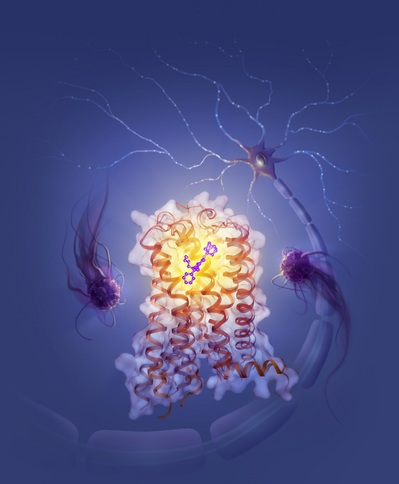
图注:与小分子AM10257结合的大麻素受体CB2和CB1,及其外周免疫细胞和神经细胞的艺术展现图,以展示其对神经和免疫系统的精准调控。

上海科技大学免疫化学研究所科研团队合影
(左起:杨秀娜、武丽杰、杨海涛、李俊、饶子和、张兵、杨扬、杨晓琳、赵耀)

上海科技大学iHuman研究所科研团队合影
(左起:武丽杰、王静静、刘志杰、华甜、李潇婷、RaymondStevens、赵素文、吴萌)




