10月19日,国际学术期刊Cell Discovery在线发表了上海科技大学免疫化学研究所杨秀娜副研究员、高岩副研究员与中国科学院上海巴斯德研究所王岚峰课题组、江陆斌课题组及复旦大学陈振国课题组的合作研究论文:The molecular mechanism of cytoadherence to placental or tumor cells through VAR2CSA from Plasmodium falciparum。

疟疾是一种由疟原虫引起,经按蚊传播的虫媒病。全球范围内,每年约2亿多人感染疟疾,导致40多万人死亡。此外,耐药虫株在不断出现,使得疟疾依然是世界上危害最大的寄生虫病。疟疾高发地区的女性在怀孕期间对疟原虫高度易感,且容易发展成凶险型胎盘相关疟疾(PAM),给孕妇及胎儿带来致命性的伤害。疟原虫编码的表达于被感染红细胞表面的VAR2CSA蛋白在PAM发生中起重要作用。疟原虫通过VAR2CSA蛋白与胎盘胚胎滋养层细胞表面的硫酸软骨素A(CSA)结合,使被感染红细胞大量粘附在胎盘,来逃避宿主的免疫识别。阻断VAR2CSA对胎盘的粘附,可以有效降低孕妇感染的风险。此外,因为恶性肿瘤组织具有和胎盘组织相同的糖基化修饰,所以VAR2CSA蛋白可以与许多不同类型的肿瘤细胞特异性结合,针对VAR2CSA的结构和功能研究也可以为肿瘤诊断与靶向性治疗提供新方案。VAR2CSA是单次跨膜的膜蛋白,在被感染红细胞表面的表达丰度较低,且全长分子量超过350 kDa,使得全长蛋白的制备难度很大,因而自该蛋白被鉴定近20年来,相关研究基本停留在各类截短突变体上。
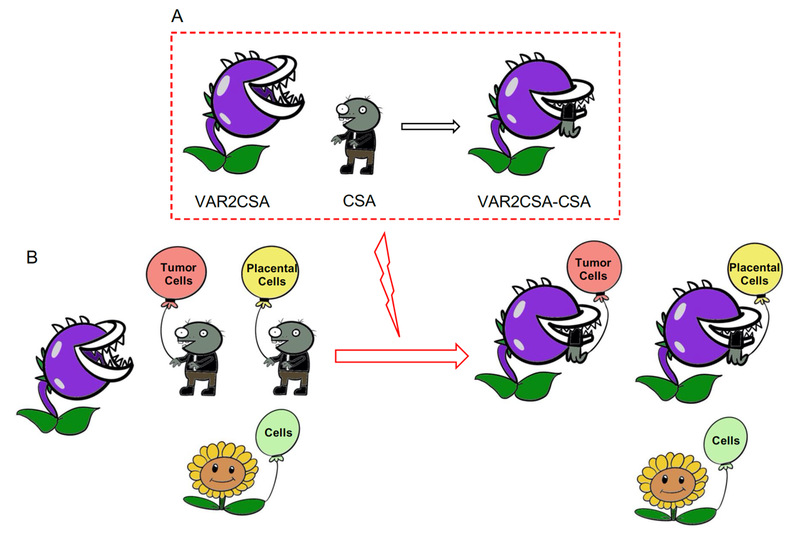
VAR2CSA 特异性识别胎盘细胞和肿瘤细胞的模型
本研究中,研究者利用杆状病毒-昆虫细胞表达系统制备了恶性疟原虫VAR2CSA胞外区的样品(306 kDa)。借助冷冻电镜单颗粒技术,解析了VAR2CSA胞外域的三维结构,分辨率为3.6Å。VAR2CSA胞外域DBL1X-DBL4ε结构域组成了一个稳定的核心区域,柔性较大的DBL5ε和DBL6ε结构域游离在核心区域外,组成了arm区。同时,研究者也成功解析了VAR2CSA胞外域-CSA复合物的结构,分辨率为3.4 Å。与Apo蛋白相比,复合物中DBL4ε的构象基本保持一致,但DBL1X和DBL2X在CSA结合到正电荷口袋后,构象发生显著变化,将正电荷口袋紧缩,从而将CSA分子稳定地捕获在由NTS,DBL1X,DBL2X和DBL4ε形成的正电荷口袋中。依据结构信息,我们选取底物结合口袋中DBL2X上的9个关键氨基酸进行突变,利用液相色谱层析,生物膜干涉技术,共聚焦免疫荧光显微技术等多种技术手段,证明了突变体失去了与纯化的CSA、胎盘及肿瘤细胞结合的能力。最终系统地阐明了恶性疟原虫VAR2CSA特异性结合胎盘细胞及肿瘤细胞的详细分子机制。该研究成果将有助于精准设计疟疾疫苗,为防治PAM提供科学依据,同时为开发高效的恶性肿瘤的诊断和靶向性治疗方法提供理论基础。
中科院上海巴斯德研究所博士研究生王伟伟和王肇宁,上科大免化所杨秀娜副研究员和高岩副研究员,复旦大学博士研究生张翔为本文的共同第一作者。上海巴斯德研究所王岚峰研究员和江陆斌研究员,以及复旦大学陈振国研究员为本文的通讯作者。该研究得到国家科技部重大专项,中国科学院战略性先导科技专项(先导B),国家自然科学基金, 上海市科技重大专项等项目的资助。冷冻电镜相关的研究得到复旦大学,上海科技大学冷冻电镜中心的大力支持。
原文链接:The molecular mechanism of cytoadherence to placental or tumor cells through VAR2CSA from Plasmodium falciparum
https://www.nature.com/articles/s41421-021-00324-8



