近日,上海科技大学免疫化学研究所姜标教授课题组联合标新生物以及免化所白芳教授团队在国际知名期刊European Journal of Medicinal Chemistry 在线发表了题为“Discovery and characterization of novel potent BCR-ABL degraders by conjugating allosteric inhibitor”的文章,报道了基于别构调节小分子抑制剂开发的新型PROTAC降解剂30(SIAIS100)可高效降解Ph+ 慢性粒细胞白血病(Chronic myeloid leukemia,CML)关键致病融合蛋白BCR-ABL,并可克服多种临床耐药相关BCR-ABL突变体,发挥了蛋白降解剂的独特作用优势。
姜标教授团队一直致力于靶向BCR-ABL小分子降解剂的设计开发,继已发表的基于BCR-ABL特异性ATP竞争抑制剂分别招募VHL (J Med Chem. 2019) 和CRBN (Eur J Med Chem. 2021)配体的两个系列的PROTACs工作后,此项工作基于变构抑制剂募集CRBN配体设计合成了新型靶向BCR-ABL的PROTACs,重点优化连接子参数以及分别跟靶点结合弹头和CRBN配体的连接位点并开展系统SAR研究,经过多轮优化筛选出最有效新型BCR-ABL降解剂30(SIAIS100)为候选化合物。
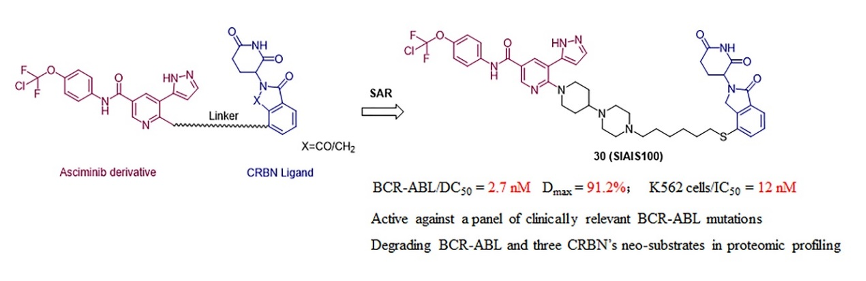
图1 靶向BCR-ABL蛋白降解剂筛选和优化
此项工作揭示候选化合物30呈现出优异的增殖抑制活性,高效的蛋白降解活性和良好的选择性;药物去除后96小时依然呈现持续长效的蛋白降解活性。
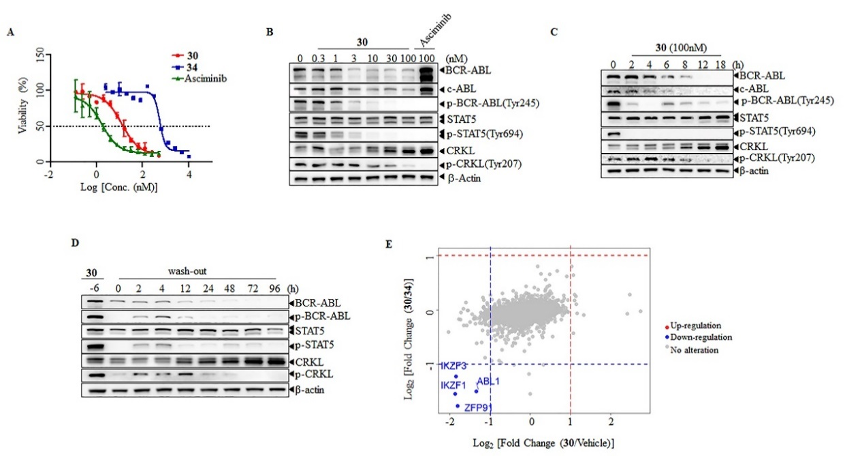
图2 化合物30对BCR-ABL蛋白的降解活性和选择性
更重要的是候选化合物30可实现一系列临床耐药相关的BCR-ABL突变体形式的高效降解。除单一突变外,30对某些高度耐药的复合突变(在同一等位基因中包含≥2个突变),特别是包含T315I的复合突变,呈现很好的降解活性,并伴随对BCR-ABL信号通路的有效抑制。
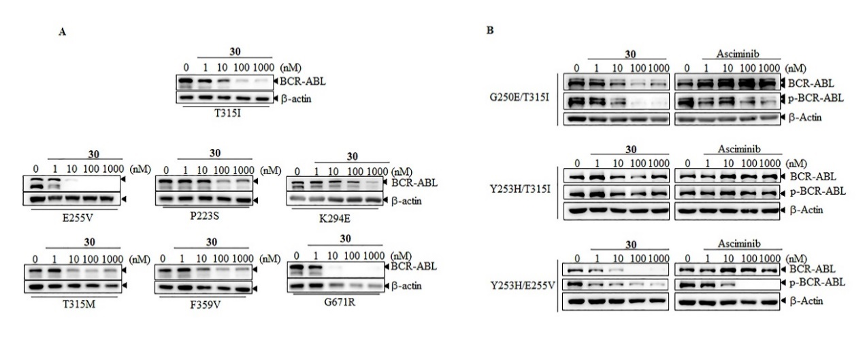
图3 降解剂30对BCR-ABL临床相关突变的降解效果
最后通过计算机模拟阐明了候选化合物30的结合作用模式,并通过多种参数开展了30诱导三元复合物的稳定性研究。结果表明与具有相似连接子长度的其他两个衍生物相比,30可诱导更稳定的三元复合体形成,从而导致更有效的BCR-ABL降解。
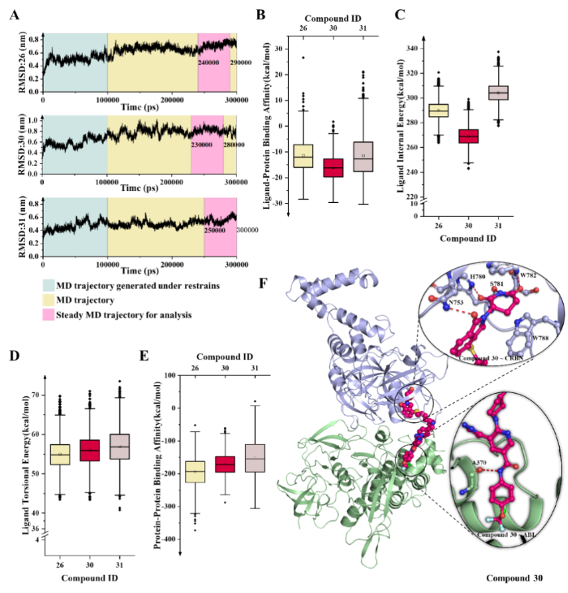
图4 降解剂30诱导的三元复合物稳定性研究
尽管靶向BCR-ABL的酪氨酸激酶抑制剂(Tyrosine kinase inhibitors,TKIs)的临床应用显著改善了Ph+ CML患者的预后,但临床治疗仍面临白血病干细胞的持续存在和临床耐药性等问题。其中主要由BCR-ABL突变导致的临床耐药已成为CML治疗的重大挑战,尤其是T315I守门员突变以及复合突变体。因此应用靶向蛋白降解的新型技术用于高效降解BCR-ABL 蛋白和其突变体形式,或可为克服CML临床治疗挑战提供新思路。
上海科技大学免疫化学研究所、生命科学与技术学院2020级博士研究生刘海霞、2018级硕士研究生米强龙、2019级博士研究生丁欣雨和2020级硕士研究生林宸岑为共同第一作者,免化所抗体化学实验室特聘教授姜标及助理研究员阴倩倩、标新生物杨小宝博士以及免化所药物设计实验室白芳教授为共同通讯作者。
本项目得到了国家自然科学基金、上海自然科学基金,上海市青年科技英才杨帆计划等项目支持,以及上海科技大学免疫化学研究所药物发现平台、分析化学平台等平台的大力支持。本项目在蛋白质表达和纯化工作中得到免化所结构生物化学实验室张贺桥副研究员和2019级博士研究生纪莉婷的大力帮助和支持。
文章链接:https://doi.org/10.1016/j.ejmech.2022.114810



