北京时间2023年9月11日晚11点,上海科技大学免疫化学研究所教授杨海涛/免化所特聘教授、清华大学教授饶子和院士团队与哥伦比亚大学何大一(David D. Ho)院士团队在国际学术期刊《自然》(Nature)上,合作发表了新冠病毒的最新研究成果“Molecular mechanisms of SARS-CoV-2 resistance to nirmatrelvir”,揭示了新冠病毒如何利用两种截然不同的途径对治疗药物产生耐药性的分子机制。

新冠病毒(SARS-CoV-2)肆虐全球,对人类健康乃至社会经济都造成了空前影响,如何开发治疗新冠的特效药是科学家们面临的极具挑战性的科学问题。目前,靶向病毒蛋白酶的药物在抗新冠药物中占有举足轻重的地位,如辉瑞公司(Pfizer Inc.)开发的新冠口服药Paxlovid(nirmatrelvir/ritonavir组合,中译名:奈玛特韦/利托那韦),以及紧急授权使用的盐野义公司(Shionogi & Co., Ltd.)的药物Xocova(ensitrelvir,中译名:恩赛特韦)等,都是靶向新冠病毒主蛋白酶(main protease,Mpro)的抗病毒药物。
随着靶向病毒蛋白酶药物的广泛使用,新冠病毒作为一种高突变的RNA病毒,是否会对Paxlovid中的抗病毒活性成分奈玛特韦产生耐药性?如果存在耐药的风险,我们将如何应对?这些都是备受关注的重要科学问题。
研究团队曾发现,在奈玛特韦的选择压力作用下,新冠病毒可以通过突变其主蛋白酶上的多个位点获得对奈玛特韦的耐药性,但其背后的精确分子机制仍是未解之谜(Iketani et al., Nature, 2022)。利用病毒主蛋白酶的结构对突变位点进行分析发现,耐药突变E166V、F140L和S144A位于主蛋白酶底物识别口袋的S1位点,L50F突变在S2位点附近,L167F和A193P突变在S4位点,而T21I突变位于S4'位点。综合利用病毒学、生物化学以及结构生物学等多学科交叉手段对以上突变展开研究,本工作首次发现了新冠病毒可以利用两种截然不同的进化途径(如图所示:Evolutionary Routes 1 & 2)对奈玛特韦产生耐药性。
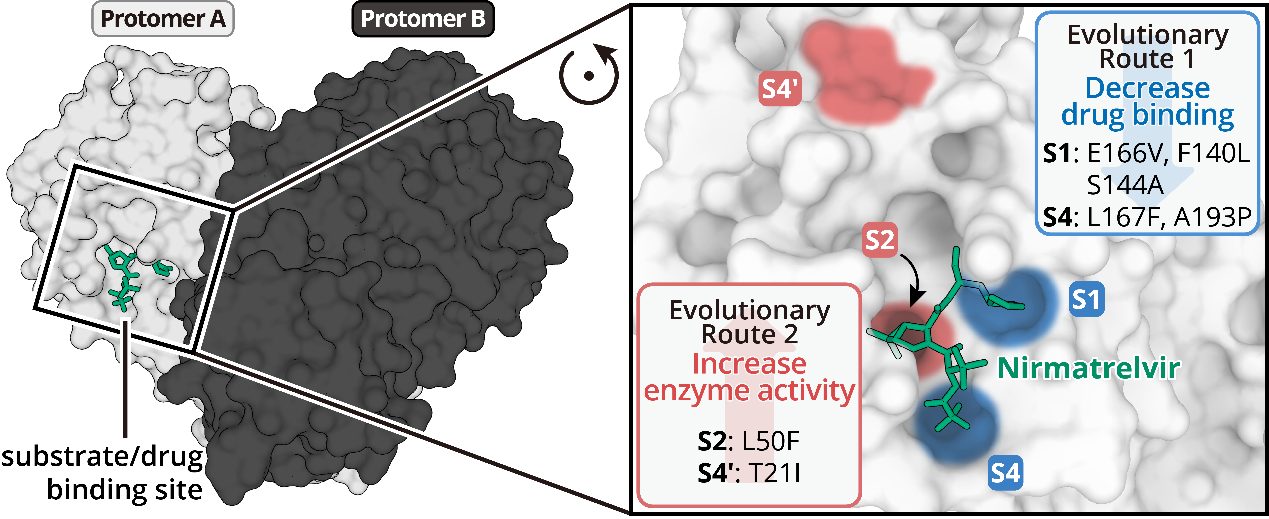
新冠病毒采取两种截然不同的进化途径对临床药物产生耐药性
第一条进化途径涉及主蛋白酶底物结合口袋的S1与S4位点,这些突变可以破坏奈玛特韦与这些位点的结合能力,削弱其对主蛋白酶活性的抑制能力。以其中最突出的E166V突变为例,这个单点突变可以严重破坏奈玛特韦与S1位点的结合,造成耐药水平增加超过200倍。但由于奈玛特韦和天然底物在蛋白酶上的结合位点高度重合,该位点突变也会严重影响病毒自身复制的速率,因此狡猾的新冠病毒同时又进化出第二条进化途径。
第二条进化途径涉及主蛋白酶底物结合口袋的S2与S4'位点,这些点突变会引起病毒主蛋白酶的活力增加。如位于S2位点的L50F突变和位于S4'位点的T21I突变,它们虽然主要并不影响奈玛特韦的结合,但却可以增强病毒主蛋白酶自身的活性。最终新冠病毒可同时采纳两种进化途径,形成T21I/E166V或者L50F/E166V双突变,在逃逸抗病毒药物攻击的同时又能够保持自身的复制和传播能力。除此之外,本工作还对另外一种靶向主蛋白酶的抗新冠药物恩赛特韦展开了研究,发现新冠病毒也可通过上述耐药机制对恩赛特韦产生耐药,这说明该耐药机制很可能具有普适性。
为了寻求解决病毒耐药的办法,研究团队进一步探索了各种小分子抑制剂与新冠病毒主蛋白酶的结合模式,发现以前报道过的一种天然产物抑制剂与蛋白酶的结合模式与上述临床药物的结合模式截然不同,而在后续的测试中也发现上述病毒的突变体尚未对该天然产物产生耐药性。这表明为了解决当前抗新冠药物在临床使用中产生潜在耐药性问题,后续可能还需要开发针对同一靶点不同结合模式的新型抑制剂,或是针对不同靶点的抑制剂,这些发现也为今后开发新一代抗病毒药物奠定了理论基础。
本项工作由上海科技大学、哥伦比亚大学、南开大学和重庆医科大学等多家单位合作完成,上海科技大学为第一完成单位。上海科技大学博士研究生段胤凯、硕士研究生周浩、南开大学副研究员刘祥、哥伦比亚大学Sho Iketani博士、重庆医科大学博士后林萌萌(上海科技大学访问学者)为论文的并列第一作者。上科大免化所和生命学院双聘教授杨海涛、哥伦比亚大学何大一院士为本论文共同通讯作者。晶体衍射数据收集在上海同步辐射光源和英国Diamond光源完成。
文章链接:https://www.nature.com/articles/s41586-023-06609-0



