上海科技大学免疫化学研究所、上海临床研究中心与复旦大学附属华山医院和德国癌症研究中心等单位紧密合作,建立了一种新型个体化患者肿瘤类器官(IPTO)模型,利用患者来源的肿瘤样本,真实再现了原发性及转移性脑肿瘤的分子病理、细胞病理和肿瘤微环境,能够精准预测患者的药物反应。近日研究成果以“Individualized Patient Tumor Organoids Fully Recapitulate Human Brain Tumor Ecosystems and Predict Patient Response to Therapy”为题,发表在国际期刊《细胞-干细胞》(Cell Stem Cell)。
肿瘤类器官是癌症研究的重要工具,但现有的脑瘤类器官模型存在一定局限,限制了其在临床反应预测中的应用。目前已建立的脑瘤类器官大多针对恶性胶质母细胞瘤,这些类器官虽然能够部分保留肿瘤的形态特征、细胞组成、基因组异常和侵袭性等,但未能充分模拟肿瘤细胞与正常脑组织之间的相互作用。此外,现有模型在体外培养后,免疫细胞及肿瘤相关免疫微环境细胞的数量显著减少,无法真实反映患者肿瘤的病理特征。而针对低级别胶质瘤及脑转移瘤的类器官体系仍为空白。
为了解决这一问题,研究团队将患者来源的原发肿瘤组织(PTs)植入由多功能诱导性干细胞(iPSC)建立的迷你大脑类器官(mini-brain)中,成功模拟了肿瘤细胞在类脑环境中的生长与侵袭。通过这一方法,研究团队建立了包含326个患者组织来源的生物样本库,涵盖了48种脑部肿瘤类型,包括各类高级别和低级别成人肿瘤、儿童肿瘤及脑转移瘤等。组织病理学、基因组学、表观遗传学以及单细胞测序分析表明,IPTO模型真实保留了患者肿瘤的细胞异质性及分子病理学特征。
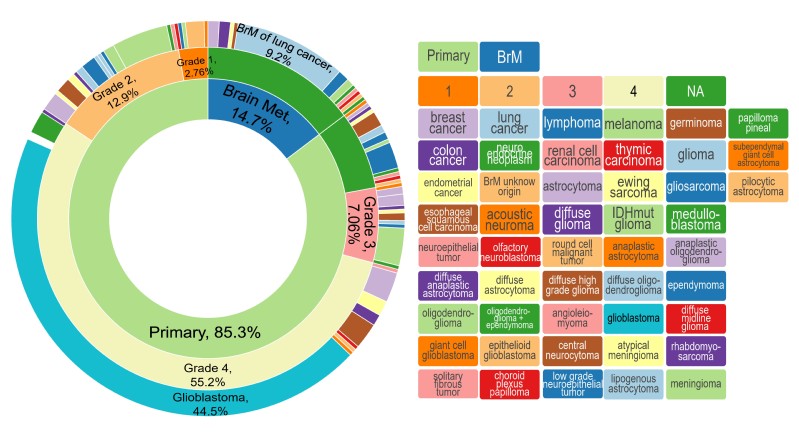
图示:该Sunburst 图展示了本研究中用于生成 IPTOs 的样本数量和肿瘤亚型占比,研究人员通过这种方法建立起326个病人组织来源的生物样本库,涵盖了48种中枢神经系统肿瘤类型,包括成人肿瘤,儿童肿瘤以及脑转移瘤等。
与传统的脑瘤类器官模型相比,IPTO模型的成功率更高,能够维持肿瘤免疫微环境特别是免疫细胞的细胞组成,并高度保持肿瘤内部的空间异质性,是目前所知唯一能够做到这一点的模型。更为重要的是,研究团队开展了一项前瞻性的临床验证,利用IPTO模型预测脑瘤患者对标准化疗药物替莫唑胺的反应,结果表明,IPTO模型能够精准预测病人反应,也表明IPTO技术成功达到了预测性临床前模型的标准。
因其独特优势及建立初就深度结合临床等特点,IPTO技术已经在中德多个医院得到快速独立验证,并且已经可以应用到化疗、靶向治疗、免疫治疗和细胞治疗药物预测。德国合作团队也已经成功把这项技术整合到TCRT临床试验流程之中。基于IPTO技术的多项国际临床应用合作也在稳步推进中。
上科大免疫化学研究所癌症干细胞课题组2022级博士研究生彭天平、德国癌症研究中心(DKFZ)麻秀建以及复旦大学附属华山医院主任医师花玮为本研究的共同第一作者。上科大免化所副研究员吴永和、特聘教授刘海坤以及复旦大学附属华山医院毛颖为本论文的共同通讯作者。
论文链接:https://www.cell.com/cell-stem-cell/fulltext/S1934-5909(25)00002-5



